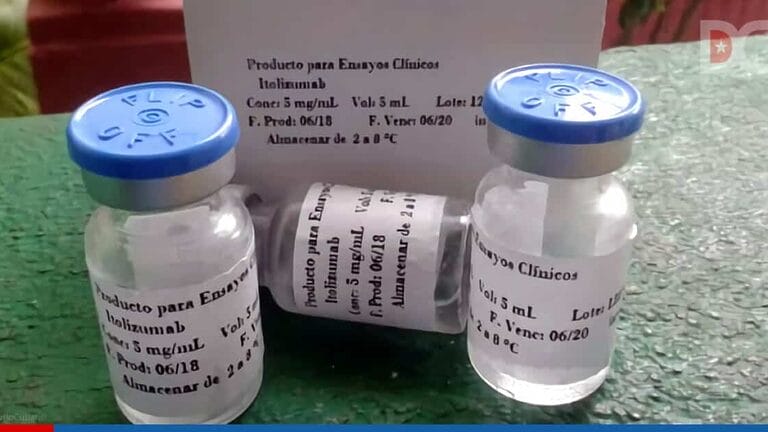
La empresa farmacéutica de la India, Biocon, ha recibido el visto nuevo para empezar a probar el anticuerpo monoclonal Itolizumab, como posible tratamiento en pacientes graves de la covid-19.
El Embajador de Cuba ante la Unión Africana anunció en su cuenta de Twitter que la India se encuentra lista para realizar ensayos clínicos en seis hospitales con el anticuerpo cubano Itolizumab, de “alentadores resultados en el tratamiento a la pandemia”.
#India is ready to conduct open trials in six hospitals of the #Cuban antibody Itolizumab to treat patients with #covid__19. The results in #Cuba are very encouraging during the pandemic. @CubaMINREX @CIGBCuba @centro_cim @lia_tadesse @AfricaCDC @AU_KwesiQuartey @JNkengasong pic.twitter.com/LitBIiyb56
— Angel Villa Hdz (@AngelVillaHdz) June 1, 2020
Según The Print, el anticuerpo monoclonal Itolizumab es una molécula que comenzó a desarrollarse conjuntamente entre la compañía farmaceútica india Biocon y el Centro de Inmunología Molecular (CIM) de Cuba.
Biocon obtuvo la licencia del medicamento del CIM, y el equipo científico de la compañía comenzó a desarrollar el anticuerpo para tratar enfermedades autoinmunes en 2006 en India. Más tarde, después de estudios exitosos con pacientes, Itolizumab fue aprobado para su comercialización en la India en 2013 para tratar la Psoriasis y se distribuyó bajo la marca ALZUMAb.
Recientemente, la empresa farmacéutica recibió el permiso de los organismos rectores en la India para reutilizar el medicamento en el tratamiento a pacientes con covid-19, de acuerdo al citado artículo.
“El itolizumab se ha utilizado en la India desde hace algunos años y se ha comprobado que es seguro. Nuestros socios en Cuba, con quienes la compañía comenzó a desarrollar el medicamento, han usado este medicamento en pacientes con covid-19. Los datos iniciales de ellos parecen bastante prometedores”, dijo a The Print el Dr. Sandeep Athalye, vicepresidente senior y director médico de Biocon Biologics.
«El fármaco inhibe la producción de citocinas proinflamatorias, lo que conduce al síndrome de dificultad respiratoria aguda y falla multiorgánica entre los pacientes de covid-19. Creemos que la ‘tormenta de citoquinas’, que es una complicación de la covid-19, puede ser tratada con Itolizumab”, agregó.
Los ensayos clínicos con el fármaco se llevarán a cabo en Nueva Delhi, Mumbai y Bangalore. Los sitios elegidos en Nueva Delhi son el All India Institute of Medical Sciences (AIIMS) y el Lok Nayak Jai Prakash Narayan Hospital, según aparece en el Clinical Trial Registry of India (CTRI).
En Bangalore, Narayana Health llevará a cabo los ensayos, y en Mumbai, KEM Hospital, B.Y.L., Nair Charitable Hospital y el Dr. Balabhai Nanavati Hospital serán los encargados.
La duración estimada de los ensayos es de tres meses.
Desde el mes de abril, el anticuerpo monoclonal humanizado Itolizumab forma parte del protocolo de atención médica a la covid-19 en Cuba.
Según Granma, el fármaco fue creado en el Centro de Inmunología Molecular (CIM) y ha sido recipiente de uno de los Premios Nacionales de la Academia de Ciencias de Cuba (ACC) en 2014, así como de la Medalla de Oro de la Organización Mundial de la Propiedad Intelectual (OMPI), en 2015.
La doctora en Ciencias Tania Crombet Ramos, directora de Investigaciones Clínicas de esa institución, perteneciente al Grupo Empresarial BioCubaFarma, comentó al diario que “el anticuerpo monoclonal se ha usado como parte de un protocolo de acceso expandido, aprobado por el comité científico conjunto entre el Ministerio de Salud Pública y el grupo empresarial BioCubaFarma para la covid-19.”
La especialista explicó que el Itolizumab, se ha empleado en pacientes clasificados como críticos, graves y de cuidado, con alto riesgo de agravamiento. “Los mejores resultados se han visto en los enfermos graves y de cuidado, donde se logra frenar a tiempo las consecuencias de la tormenta de citocinas. Igualmente, en muchos casos hay evidencias clínicas e imagenológicas del mejoramiento del distrés respiratorio.”
Al tratarse de ensayos clínicos abiertos, desde la India aclaran que no se ocultará ninguna información a los investigadores y participantes sobre el curso del tratamiento administrado.
De acuerdo con los detalles del ensayo publicado en el portal del Clinical Trial Registry of India y citado en The Print, todos los pacientes elegibles que ingresen al estudio serán asignados al azar en una proporción de 2: 1 para recibir el tratamiento A y B, respectivamente. Esto Significa que el grupo A tendrá el doble de personas que el grupo B.
El tratamiento del grupo A recibiría un tratamiento con Itolizumab, mientras que el B recibiría otras terapias que incluyen el uso de antivirales, antibióticos, hidroxicloroquina u oxigenoterapia.
Seguir leyendo en Directorio Noticias
Sigue nuestros canales de WhatsApp, Telegram y Facebook.
 Nota informativa de la Unión Eléctrica de Cuba
Nota informativa de la Unión Eléctrica de Cuba  Nota informativa de CUPET sobre el suministro de gas a la población
Nota informativa de CUPET sobre el suministro de gas a la población  Cuba: anuncian cierre de Embajada en La Habana por varios días. Se paralizan trámites
Cuba: anuncian cierre de Embajada en La Habana por varios días. Se paralizan trámites